| [chimie organique] déterminer une formule brute par microanalyse [63234] |
|
| Posté le : 19/01/2009, 08:26 (Lu 14906 fois) |
Bonjour, j'ai un gros soucis pour demarer un exos de chimie organique et ça m'handicap pour la suite. Voici la partie de l'enoncé qui coince :
DÉTERMINATION DE LA STRUCTURE DE L’ alpha-IRONE [ Je n'aiu pas du tout de formule]
La microanalyse quantitative (oxydation totale par l’oxydation de cuivre II dans un courant de
dioxygène), effectuée sur un échantillon de masse mo = 10,32 mg, fournit m1 = 30,83 mg de
dioxyde de carbone CO2 et m2 = 9,91 mg d’eau. [ Je précise que je ne connais pas du tout cette technique ]
La masse molaire de l’ alpha -irone est M = 206 g.mol-1.
I.1.a) En supposant que la molécule d’ alpha-irone ne contient que du carbone, de l’hydrogène et de l’oxygène, déterminer la formule brute de l’ alpha-irone .
I.1.b) Déterminer le degré d’insaturation que présente la molécule.
| |
|
|
| Re: [chimie organique] déterminer une formule brute par microanalyse [63235] |
|
| Posté le : 19/01/2009, 12:18 (Lu 14898 fois) |
Bonjour,
Le plus souvent on brûle une substance dans du dioxygène à volonté et on obtient du CO2 (gaz carbonique), du H2O (vapeur d'eau), et d'autres choses si la molécule contient autre chose que du C, du H et du O.
De la masse de CO2, tu peux déduire la masse de carbone que contenait la totalité de la masse de ta substance.
De la masse de H2O, tu peux déduire la masse d'hydrogène...
Tu connais les masses molaires de CO2 et H2O, donc tu peux en déduire les quantité de matière (nombre de mole) de C et H.
Tu connais aussi la masse molaire de ta substance, l'alpha-irone et la masse de cette substance qui a servi à l'analyse.
Alors est-ce cela peut te mettre sur la voie ?
| |
|
|
| Re: [chimie organique] déterminer une formule brute par microanalyse [63239] |
|
| Posté le : 19/01/2009, 17:13 (Lu 14890 fois) |
Il faut que je suppose que n(CO2)=n(C) alors ?
Dans ce cas je vois comment faire.
n(C) =m(CO2)/M(CO2).
Je multiplie n(C)par 12 et que je divise par mo. n(C)*12/mo
Ca me donne le pourcentage de C dans la molécule que je multiplie par M(alpha iranone). Ca me fait 14 carbonnes dans la molécules ce qui est vraissemblable.
MAIS, si j'applique le même raisonnement pour trouver H, c'est à dire
n(H2O)=n(H) j'ai un chiffre abberant à la fin.
Comme dans H20 il y a deux hydrogéne j'ai essayé en faisant n(H20)/2 = n(H). Mais ça ne marche pas non plus ! Ou est ma faute alors ?
| |
|
|
| Re: [chimie organique] déterminer une formule brute par microanalyse [63242] |
|
| Posté le : 19/01/2009, 17:40 (Lu 14888 fois) |
Pas mal !
Citation : Ayuda
MAIS, si j'applique le même raisonnement pour trouver H, c'est à dire
n(H2O)=n(H) j'ai un chiffre abberant à la fin.
Comme dans H20 il y a deux hydrogéne j'ai essayé en faisant n(H20)/2 = n(H). Mais ça ne marche pas non plus ! Ou est ma faute alors ?
|
|
Imaginons qu'une molécule de CH4 brûle dans le dioxygène pour conduire à 2 molécules d'eau et une de CO2.
Remplaçons le mot "molécule" par "mole".
Tu obtiens 2 mol de H2O. Et dans ta molécule de départ du avait 4 mol de H.
N'as-tu pas divisé par 2 au lieu de multiplier ? 
| |
|
|
| Re: [chimie organique] déterminer une formule brute par microanalyse [63243] |
|
| Posté le : 19/01/2009, 17:51 (Lu 14886 fois) |
D'accord, j'ai compris   . Merci beaucoup ! . Merci beaucoup !
| |
|
|
| Re: [chimie organique] déterminer une formule brute par microanalyse [63247] |
|
| Posté le : 19/01/2009, 20:23 (Lu 14877 fois) |
Bin alors ? Quelle est la réponse ?
| |
|
|
| Re: [chimie organique] déterminer une formule brute par microanalyse |
|
| Posté le : 20/01/2009, 10:18 (Lu 14867 fois) |
14 C, 22H et 1 0xygéne. Du coup, 4 insaturations (14*2+2 H théorique - 22 H effectifs)/2. 
Merci pour les conseils et explications ! 
| |
|
|
| Re: [chimie organique] déterminer une formule brute par microanalyse [63267] |
|
| Posté le : 20/01/2009, 23:57 (Lu 14852 fois) |
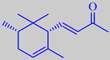
| |
|
|
| Re: [chimie organique] déterminer une formule brute par microanalyse [63277] |
|
| Posté le : 21/01/2009, 12:31 (Lu 14848 fois) |
Whaou ! Super, merci !
| |
|
|
Aztek Forum V4.00 Copyright (C) 2003 |